ОПИСАНИЕ ИЗОБРЕТЕНИЯ К ПАТЕНТУ
Свищи – причина рака толстой кишки.
Изобретение относится к медицине, в частности к абдоминальной хирургии, и может быть использовано для лечения воспалительного процесса в области анастомоза после резекции желудка.
Известен способ лечения анастомозита после резекции желудка, предусматривающий парэнтеральное введение раствора питательных веществ и эвакуацию застойного содержимого желудка [1] . Однако лечение анастомозита по этому способу требует не менее двух недель, а при тяжелых формах анастомозита трудно переносится больным и иногда требует повторной операции.
Известен также способ лечения анастомозита после резекции желудка, заключающийся в введении в культю желудка депо-формы противомикробного средства и фиксации ее в области анастомоза [2]. Однако применение этого способа ограничено тем, что многие известные на сегодняшний день противомикробные средства оказывают действие на ферментативные функции тканей макроорганизма и поэтому могут оказывать на него токсическое действие.
Наиболее близким по технической сущности к предлагаемому изобретению является способ лечения анастомозита после резекции желудка, предусматривающий удаление застойного содержимого и ведение в культю желудка раствора противовоспалительного средства [3].
В этом способе в качестве противовоспалительного средства используют 20%-ный раствор сорбитола, который представляет собой шестиатомный спирт. При попадании в организм за счет всасывающей способности слизистой желудка сорбитол, благодаря своей высокой биологической активности, претерпевает метаболические превращения, окисляясь до сорбозы, и теряет свои противовоспалительные свойства.
Поэтому при лечении воспалительного процесса по существующему способу требуется неоднократное (до 8-ми доз) введение сорбитола в культю желудка, что удлиняет срок купирования процесса.
Техническая задача предлагаемого изобретения заключается в сокращении срока лечения анастомозита.
Поставленная задача достигается тем, что в известном способе лечения анастомозита после резекции желудка, предусматривающем удаление застойного содержимого и введение в культю желудка раствора противовоспалительного средства, в качестве противовоспалительного средства используют перфторуглеродную эмульсию, например, «Перфторан» [4].
Указанные особенности предлагаемого изобретения представляют его отличие от прототипа и обуславливают новизну предложения. Эти отличия являются существенными, поскольку именно они обеспечивают создание достигаемого технического результата, отраженного в технической задаче, и отсутствуют в известных технических решениях с тем же эффектом.
Впервые возникновение пептической язвы после гастроэнтеростомии описал Н. Braun в 1899 г., а после резекции желудка – Н. Haberer в 1929 г. В литературе за последние 20 лет авторы приводят частоту постгастрорезекционных пептических язв от 1 до 4% [3]. 90 — 98% пептических язв соустья развиваются после резекции, выполненной по поводу язвы двенадцатиперстной кишки. Это связывают с тем, что дуоденальные язвы, как правило, сопровождаются желудочной гиперсекрецией и гиперхлоргидрией, а сохранение секреторной функции культи желудка на уровнях, сравнимых с дооперационными, и является основной причиной развития пептической язвы.
Выделяют четыре основные причины сохранения кислотопродукции в культе желудка: 1) экономная резекция (менее 2/3) без ваготомии, с сохранением кислотопродуцирующей зоны; 2) оставление части антральной слизистой оболочки на культе двенадцатиперстной кишки при резекции по второму способу Бильрота; 3) гипертонус блуждающих нервов и неполная ваготомия, если она выполнялась в сочетании с экономной резекцией желудка; 4) эндокринные заболевания – первичный гиперпаратиреоидизм, синдром Золлингера-Эллисона, синдром Вермера и др. Из указанных причин чаще всего встречаются первые две. Они являются техническими погрешностями операции. Самая распространенная ошибка – экономная резекция желудка при язве двенадцатиперстной кишки без ваготомии.
Она не только не снижает повышенной кислотности и пептической активности желудочного сока, но и создает условия для постоянного воздействия агрессивного желудочного содержимого на слизистую оболочку тощей или двенадцатиперстной кишки в результате удаления привратника. Другая характерная ошибка – оставление части антрального отдела на культе двенадцатиперстной кишки. Чаще всего это бывает при резекции на выключение, когда не иссекается антральная слизистая оболочка в оставляемом участке желудочной стенки. Выключенный из тока кислого желудочного содержимого антральный отдел при этом является постоянным источником гастринемии, причем уровни сывороточного гастрина могут быть при этом так велики, а течение болезни так жестоко, что отличить эту патологию от синдрома Золлингера-Эллисона до операции можно только по результатам определения уровней гастрина с применением секретинового теста. Причины гипергастринемии при отключенном антральном отделе – в отсутствие тормозящего действия хлористоводородной кислоты на гастринпродуцирующие клетки антральной слизистой оболочки и в вагусной денервации [1].
Сведения о гипертонусе блуждающих нервов как причине сохранения кислотопродукции в культе желудка в литературе немногочисленны. Замечено, что даже при значительных по объему резекциях и отсутствии эндокринных расстройств у 5-10% больных кислотность остается высокой. Попытки выделить группу больных с гипертонусом блуждающих нервов по различным секреторным тестам, в том числе и с ложным кормлением, вряд ли могут значительно помочь хотя бы из-за трудностей интерпретации результатов в условиях резецированного желудка (с одной стороны, быстрая эвакуация кислоты, с другой – заброс щелочного кишечного содержимого в культю желудка). Тем не менее, на основании благоприятных непосредственных и отдаленных результатов изолированной ваготомии при пептических язвах можно сделать вывод о наличии у таких пациентов гипертонуса блуждающих нервов [1].
Следующая группа причин пептической язвы — эндокринные заболевания. Встречаются они редко, но значение их определяется, например, тем фактом, что больные с синдромом Золлингера-Эллисона имеют в анамнезе операцию и страдают рецидивной язвой. По некоторым данным, у 75% больных с синдромом Золлингера-Эллисона язвы имеют типичную локализацию, при этом может не быть ни клинических, ни лабораторных специфических признаков. Попытки рентгенологической диагностики синдрома основываются на ряде признаков: 1) большой атоничный желудок с грубыми складками или гиперсекреция в маленькой культе; 2) большая атоничная двенадцатиперстная кишка; 3) усиленная перистальтика, быстрый пассаж по тонкой кишке, отек слизистой оболочки; 4) необычная локализация язвы с признаками пенетрации. Единственным достаточно точным методом дооперационной диагностики синдрома Золлингера-Эллисона является радиоиммунологическое исследование уровней гастрина в периферической крови.
Другой важный вопрос при выявлении синдрома Золлингера — Эллисона состоит в локализации источника гипергастринемии до операции, так как это может радикально изменить лечебную тактику. Дело в том, что, во-первых, различают два типа синдрома Золлингера-Эллисона: тип 1–без опухоли вообще, обусловленный гиперплазией гастринпродуцирующих клеток антрального отдела желудка, и тип 2–когда источник гастрина (опухоль-гастринома) локализуется вне антрального отдела. При первом типе можно добиться излечения применением простой резекции желудка с ваготомией. Трудности локализации гастрином при втором типе состоят в том, что опухоль может быть микроскопической (в стенке двенадцатиперстной кишки), множественной, злокачественной и давать метастазы, которые также продуцируют гастрин.
При синдроме Вермера чаще всего поражаются паращитовидные железы, поджелудочная железа, гипофиз, надпочечники, реже щитовидная железа. При синдроме Сиппла развивается медуллярная карцинома щитовидной железы, медуллярная феохромоцитома и гиперпаратиреоидизм; при синдроме Шимке – то же самое, плюс выступающая челюсть, толстые губы, марфаноподобный вид, множественные невриномы на слизистых оболочках, гастроинтестинальный нейроматоз, плоскостопие. Гиперпаратиреоидизм, входящий в понятие полиэндокринного аденоматоза, может быть первичным и также приводить к возникновению желудочных и дуоденальных язв. Непаратиреоидные опухоли (в том числе и гастринома) могут продуцировать паратгормон и тем самым вызывать гиперкальциемию и гипофосфатемию. В дифференциальной диагностике первичного гиперпаратиреоидизма в этом случае может помочь только селективная катетеризация сосудов с забором крови непосредственно от паращитовидных желез и определением в ней уровня паратгормона [1].
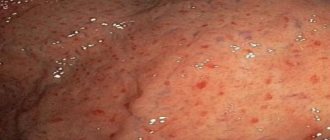
При типичной клинической картине диагностика пептической язвы не сложна. Сильные голодные (в том числе ночные) боли в эпигастральной области, уменьшающиеся после еды или приема соды, атропина, тошнота и рвота (каловая при осложнении язвы развитием желудочно-ободочного свища), поносы, похудание, рецидивирующее желудочно-кишечное кровотечение позволяют заподозрить наличие язвы в желудочно-кишечном анастомозе [1-3]. Зачастую пептические язвы протекают гораздо более злокачественно, чем первичная язва, по поводу которой была предпринята операция. Пептические язвы располагаются, как правило, на кишечной стороне гастроэнтероанастомоза, вблизи брыжеечного края кишки, что объясняет склонность таких язв к кровотечению, которое бывает часто очень сильным. Нередко одновременно существуют две язвы в области анастомоза (рис.).
Рис. Две пептические язвы, выявленные при эндоскопическом исследовании области желудочно-кишечного анастомоза
Эти язвы достигают иногда больших размеров, они пенетрируют в соседние органы и ткани (брыжейку тонкой и ободочной кишки, поджелудочную железу, печень, диафрагму), что объясняет часто очень выраженный болевой синдром.
Однако клиника может быть и не такой яркой. Боли могут быть умеренными или даже отсутствовать вовсе. В таких случаях пептическая язва проявляется обычно желудочно-кишечным кровотечением.
Рентгенологическая диагностика пептической язвы сложна и выявляет в среднем 50-65% от всех язв анастомоза. Это связано с наличием в области анастомоза различных деформаций и карманов, в которых может маскироваться язва и которые в свою очередь могут симулировать ее.
Лучше всего выявляются пептические язвы при эндоскопическом исследовании, но и эндоскопия может мало помочь, если не удается пройти аппаратом в приводящую или отводящую петлю, т. е. ниже анастомоза. При эндоскопическом исследовании в подавляющем большинстве случаев язва обнаруживается на приводящей или отводящей петле тонкой кишки.
В ряде случаев при яркой клинической картине и при обнаружении гиперацидности в культе желудка сама язва не выявляется ни рентгенологически, ни эндоскопически, а иногда даже и на операции. Пептическая язва иногда может быть поверхностной, легко заживать от консервативного лечения, но затем быстро рецидивирует, давая подчас осложнения, чаще всего кровотечение [1].
Консервативное лечение пептической язвы анастомоза включает назначение больным блокаторов Н2-рецепторов, ингибиторов протоновых помпов. При подозрении на H. pylori назначаются антибиотики. Большинство больных поддаются медикаментозному лечению. Хирургическое лечение показано больным, для которых консервативная терапия малоэффективна, при гастриноме, при таких осложнениях как профузное кровотечение, перфорация, сужение анастомоза, желудочно-ободочный свищ [3].
Повторные операции на желудке и кишечнике при язвенной болезни предпринимаются нечасто и являются сложными вмешательствами. Из большого числа операций, предложенных для лечения болезней оперированного желудка, можно выделить две основные группы: одна направлена на ликвидацию всевозможных функциональных (патофизиологических) или механических расстройств – так называемые корригирующие операции; вторая преследует цель удаления пораженной части или целого органа. Важным моментом и при тех, и при других операциях является создание условии для пищеварения, максимально приближенных к физиологическим, для чего, например, стремятся восстановить дуоденальный пассаж путем реконструкции анастомоза по Бильрот I или за счет использования одного из вариантов гастроеюнодуоденопластики [1].
Диапазон операций, применяемых при пептической язве желудочно-кишечного соустья, довольно широк. Это и ререзекция по обоим способам Бильрота в различных модификациях, ваготомия стволовая (трансторакальная и поддиафрагмальная) и селективная желудочная, а также различные сочетания ваготомии и ререзекции.
Выбор операции при пептической язве зависит прежде всего от ее причины. В этом смысле большое значение приобретает полноценное предоперационное обследование, которое должно обязательно включать, например, определение уровней гастрина в сыворотке крови, чтобы не пропустить синдром Золлингера-Эллисона. Например, самой простой операцией при пептической язве является трансторакальная ваготомия. Она эффективно снижает желудочную секрецию и способствует быстрейшему заживлению язвы. Но эта операция не позволяет выполнить необходимое корригирующее вмешательство на органах брюшной полости, например, при вторичном синдроме приводящей петли за счет пептической язвы или при сопутствующем демпинг-синдроме.
Ререзекция культи желудка необязательна, если она маленькая – в таких случаях ваготомия (и, если нужно, удаление оставленного антрального отдела) оказывает быстрый и стойкий лечебный эффект. Удаление самой язвы принципиально необязательно, но вопрос этот в каждом конкретном случае решается индивидуально – при большой пенетрирующей язве, резко деформирующей и стенозирующей зону анастомоза, лучше выполнить ререзекцию, хотя мобилизация культи желудка в таких условиях всегда достаточно сложна. Кроме того, нельзя полностью исключить опасность возникновения кровотечения из оставленной язвы в ближайшем послеоперационном периоде.
При большой желудочной культе (после экономной резекции 1/2 желудка или антрумэктомии) необходима ререзекция культи желудка. Но если предыдущая операция сделана по первому способу Бильрота, можно ограничиться ваготомией. Необходимо отметить, что после резекции по Бильрот I пептические язвы бывают гораздо реже, чем после резекции по Бильрот II, но протекают также тяжело, с пенетрацией, повторными кровотечениями и выраженным болевым синдромом. Если делать при них ререзекцию, могут возникнуть те же трудности с обработкой двенадцатиперстной кишки, как и при низких пенетрирующих дуоденальных язвах. В таких ситуациях селективная проксимальная ваготомия (СПВ) является методом выбора.
Гастрэктомия остается методом выбора при синдроме Золлингера-Эллисона. При выявлении синдрома Золлингера-Эллисона у больного с дуоденальной язвой в настоящее время большинство хирургов склоняются к более консервативному подходу. Предлагается два основных хирургических метода: 1–лечение блокаторами желудочной секреции, затем резекция желудка в сочетании с ваготомией, затем опять длительное, иногда пожизненное лечение блокаторами Н2-рецепторов; 2–сначала лечение блокаторами Н2-рецепторов, затем СПВ, затем снова блокаторы Н2-рецепторов. При обнаружении солитарной аденомы все предпочитают ее удалять.
Пептические язвы при гиперпаратиреоидизме и синдроме Вермера должны лечиться иссечением гормонально-активных тканей (паратиреоидэктомия или субтотальная резекция паращитовидных желез).
Наиболее тяжелые ситуации встречаются при осложнении пептической язвы перфорацией или профузным кровотечением. Естественное желание быстрее завершить экстренную операцию может приводить к техническим ошибкам. Конечно, в условиях выраженного спаечного процесса, пенетрации язвы и при тяжелом общем состоянии больного делать реконструктивную ререзекцию не стоит. Методом выбора в таких случаях являются ушивание язвы и стволовая ваготомия. После выведения больного из тяжелого состояния его необходимо полноценно обследовать и решить вопрос о дальнейшем лечении, возможно, о новой реконструктивной операции [1].
Нами проведен анализ историй болезней 5 больных с диагнозом пептическая язва желудочно-кишечного анастомоза, госпитализированных в отделении хирургической гастроэнтерологии клинической больницы N 3 г. Еревана с апреля 1987г. по август 2000г. Все больные – мужчины в возрасте от 35 до 54 лет. У 2 больных пептическая язва анастомоза была осложнена кровотечением, а у одного больного имелись синдром приводящей петли и желчнокаменная болезнь. Больные перенесли резекцию желудка по Бильрот II по поводу язвенной болезни двенадцатиперстной кишки (3 больных) или желудка (2 больных). Больные предъявляли следующие жалобы: боли в эпигастральной области (5 больных), тошнота (3), рвота (3), чувство дискомфорта в животе (3), общая слабость (2), отрыжка (1), боль в правом подреберье (1 больной). У больных с кровоточащей пептической язвой анастомоза была боль в эпигастральной области, общая слабость, тошнота, рвота кофейной гущей, дегтеобразный стул, чувство дискомфорта в животе. Вышеуказанные жалобы у больных появились от 4 месяцев до 8 лет после резекции желудка по Бильрот II.
Пептическая язва анастомоза у больных была установлена эндоскопически, в течение нескольних часов с момента поступления в клинику. При эзофагогастродуоденоскопии (ЭГДС) у больных с пептической язвой на стенке анастомозированной петли тонкой кишки были обнаружены язвы величиной 0,3-2,5см. В одном случае при эндоскопии был выявлен рефлюкс желчи из приводящей петли тонкой кишки в культю желудка. Все больные получили консервативное лечение, некоторые отказались от предложенной операции и были выписаны из стационара с улучшением в сроки от 2 до 24 дней.
Таким образом, ЭГДС является наиболее достоверным способом диагностики пептической язвы анастомоза. Эндоскопическое исследование дает возможность также с достоверностью судить о размерах культи желудка, т. е. в ряде случаев выявляет причину возникновения пептической язвы.
Литература
- Черноусов А.Ф., Богопольский П.М., Курбанов Ф.С. Хирургия язвенной болезни желудка и двенадцатиперстной кишки. М., 1996, с. 202-208.
- Christiansen S., Ram M., Sachatello C., Griffen W. Management of gastrocolic fistula. Am. Surg. 1981; 47. p. 63-66.
- Glasgow R.E., Mulvihill S.J. Postgastrectomy syndromes. 1997, p. 149-150.
Виды стом
Стеноз разделяют на 3 основных типа. Классификация зависит от места, где расположено сужение.
В зависимости от патологии врач подбирает наиболее оптимальный способ лечения. По мере возможности хирург всегда пытается сохранить большую часть органа.
гастростома;кишечные: илеостома, колостома;трахеостома;эпицистостома.
По форме бывают выпуклые и втянутые. Существуют одноствольные и двуствольные. В зависимости от длительности применения: временные и постоянные.
В соответствии с локализацией колостомы классифицируются на несколько типов: поперечную, восходящая и нисходящая.
Поперечная колостома.
Трансверзостому формируют в верхней зоне живота, в поперечном ободочнокишечном отделе.
Чтобы избежать нервных повреждений поперечную стому располагают ближе к селезеночному левому изгибу.
Показана поперечная колостома при кишечной закупорке или онкопатологиях, травматических повреждениях и дивертикулитах, врожденных толстокишечных аномалиях.
Местоположение колостомы определяет врач с учетом конкретной клинической картины каждого пациента.
Наиболее часто встречающийся вид тонкокишечной непроходимости – это непроходимость при спаечной болезни. Для толстой кишки – это перекрытие просвета кишки опухолью.
Спаечная кишечная непроходимость
Виды, этапы, инструментарий
Понятие гастрэктомия обозначает полное удаление желудка. Но разработаны разные этапы техник, позволяющие сохранить фрагменты органа. Поэтому выделяют виды операции:
- Дистальная субтотальная – удаляется часть, присоединённая к кишечнику;
- Проксимальная субтотальная – удаление фрагмента в верхней трети с сальниками и лимфоузлами;
- Тотальная – полное удаление с последующим формированием анастомоза;
- Рукавная – для борьбы с ожирением, удаление тела и дна желудка, сшивание узкого канала. После операции пациент съедает меньше, так как быстро приходит ощущение наполненности органа.
Субтотальная резекция проводится с пластикой тонкой кишки.
Операция проходит в 4 стадии:
- Разрез в полости живота;
- Осмотр состояния желудка – хирург устанавливает, где находится опухоль;
- Мобилизация желудка;
- Анастомоз – соустье закрепляется в плотный узел, чтобы соединение не разошлось.
Оперативная хирургия при резекции желудка применяет следующие инструменты:
- Набор для лапаротомии – для рассечения брюшной полости;
- Жомы, расширители;
- Диссектор;
- Зажимы.
Инструменты применяются также при язвенной болезни.
Симптоматика
Согласно наиболее распространенной в настоящее время классификации такие расстройства могут быть подразделены на
- органические,
- функциональные
- и сочетанные осложнения после резекции желудка.
Функциональные расстройства после резекции желудка включают: ранний и поздний (гипо-гипергликемический) демпинг-синдромы и условно — синдром приводящей петли, обусловленный нарушением эвакуаторной ее деятельности (он иногда имеет и органическую обусловленность), постгастро-резекционную астению (дистрофию) и анемию.
Симптомы хронического синдрома приводящей петли после удаления желудка
Хронический синдром приводящей петли подразделяют на
Стеноз у взрослых проявляется практически той же симптоматикой, что и у детей. Но у взрослых симптоматика более затяжная, ярко выраженная.
В начале болезни пациенты начинают страдать в основном от сильнейшей боли в верхней части живота.
Сразу после прибавляется тошнота, рвотные рефлексы и непосредственно сама рвота. Рвать пациент обычно начинает сразу после приёма пищи, массы могут содержать в себе примесь желчи.
Стеноз очень часто имеет и такое проявление, как практически полное отсутствие стула. Так как организм больного не получает необходимого количества жидкости, человек страдает и от обезвоживания. Постепенно количество мочи уменьшается до такой степени, что организм сталкивается с анурией.
При врожденном стенозе симптоматика сразу же проявляется ярко. Дети, в первую очередь, страдают от обильной рвоты. Проявиться рвота может даже до момента начала кормления малыша. Состояние детей со стенозом постоянно ухудшается.
Рвота со временем проявляется ещё более агрессивно, в ней появляются примеси фекалий и крови, запах становится крайне неприятным, кислым.
Главный симптом недуга, это появление рвоты, которая наблюдается сразу после рождения ребёнка (в первые дни рождения). Рвота может появится до кормления грудью. При стенозе рвотные массы слизистые или же водянистые.
Заболевание дает о себе знать повторением болей вверху живота, прослеживается рвота и тошнота. Рвота может начинаться сразу после принятия пищи или без причины.
В извеграемых массах можно заметить много желчи. Естественный стул отсутствует.
Человек меняется по внешнему виду — пересыхает и приобретает сероватый оттенок кожа. Это объясняется тем, что организму не хватает жидкости.
Со временем симптомы ухудшаются, рвотные массы приобретают неприятный запах из-за примесей фекалий и крови. Живот постоянно вздут, частые обмороки, приступы удушья, нехватка воздуха и головокружения.
Все это признаки стеноза.
У детей с врожденной аномалией в виде стеноза, после рождения начинается рвота. Рвотные массы приобретают зеленого цвета из-за желчи. Эти симптомы появляются спустя короткое время после рождения ребенка. Можно определить болезнь по другому характерному признаку — отсутствие стула у появившегося на свет младенца. Причиной является сужение просвета толстой кишки.
Клинические проявления. Заболевание проявляется весьма характерными симптомами.
Это боли в животе схваткообразного характера, вздутие, тошнота, рвота, не отхождение газов, отсутствие стула, нарушение общего состояния. Клиническая форма заболевания может быть острой, когда все перечисленные симптомы резко выражены, и хронической, при которой они проявляются периодически и нет резких нарушений общего состояния.
Образ жизни после резекции
На восстановление и реабилитацию требуется от полугода до года. После удаления желудка при раке, в первые 2-3 суток пациенту требуется особый уход. Питание производится через зонд и внутривенно. Жидкость восстанавливается также через вену.
Затем начинается период самостоятельного питания. Огромную роль играет диета. Сколько можно есть и что можно есть определяет врач. Однако можно дать некоторые общие рекомендации по питанию.
- Съедать нужно минимальные порции еды. Так кишечник не будет перегружаться, и самочувствие пациента не будет ухудшаться.
- Питание должно быть дробным. Кушать нужно часто и малыми порциями. Следует есть по 6-9 раз в течение дня.
- В пищу разрешается употреблять фрукты, овощи, каши и т. д. Все продукты должны быть протертыми, приготовленными на пару.
Масса тела при таком питании падать до критических отметок не будет. Набирать ее не требуется, поэтому вопрос, как набрать вес, излишен. Он будет на стабильном уровне, главное составить полноценную диету. Этот вопрос решается в индивидуальном порядке с врачами гастроэнтерологом и диетологом.
Диагностика
Диагностирование стеноза происходит с учетом сбора анамнеза, истории болезни, а также на основе инструментальных и лабораторных исследований.
Для точного диагностирования болезни применяют обширное исследование брюшной полости.
Чтобы поставить точный диагноз проводят обширное медицинское обследование. Для диагностики используются новые лабораторные тесты и инструментальные процедуры (рентген с использованием контрастных веществ, УЗИ брюшной полости и толстой кишки).
Диагностическая схема подбирается с целью определения, насколько сильно прогрессировала болезнь и какими методами ее лучше лечить, чтобы не навредить человеку.
Как проводится гастроэктомия
Ход операции при гастроэктомии предусматривает выполнение разреза на нижнем конце двенадцатиперстной кишки, а также ее удлинение навстречу к пищеводу. Окончание 12-перстной кишки соединяется непосредственно с тонкой кишкой. Продолжительность операции обычно не превышает 5 часов, а после резекции желудка требуется пребывать в стационаре на протяжении не менее 2 недель.
Реабилитация после рака желудка основывается на воздержании от употребления продуктов питания и напитков на протяжении 3-5 дней. Обновленная пищеварительная система может представлять собой смертельную опасность, если произойдет утечка соединения прямой кишки с пищеводом.
Важно знать! Для проверки на утечки прибегают к такому методу, как рентгеновское облучение. Последствия могут быть самыми разнообразными, поэтому следует воздержаться от употребления пищи и воды.
Лечение
Новорождённым детям при обнаружении стеноза требуется немедленное хирургическое вмешательство. Длительность операции во многом зависит от участка локализации патологического процесса. Больному перед хирургическим вмешательством необходимо очистить пищеварительный тракт от лишней жидкости и газов. С этой целью через рот вводится тонкая трубочка, позволяющая эвакуировать жидкое содержимое ЖКТ.
Лечение детей
И острая, и хроническая формы болезни в большинстве случаев лечатся хирургическим методом. Лишь в самом начале заболевания, когда общее состояние больного еще не нарушено, после обследования осторожно применяют консервативные меры – промывание желудка, очистительные клизмы, при атонии проводится стимуляция перистальтики препаратами (инъекции прозерина, неостигмина).
Если в течение нескольких часов проводимое лечение неэффективно или причиной является опухоль, спайки, аномалии, брыжеечный тромбоз, проводят хирургическое лечение.
Лимфодиссекция при раке желудка
Данная процедура считается обязательной при всех радикальных воздействиях на основной пищеварительный орган. Выполняется она по значимым соображениям и не имеет никакой взаимосвязи с наличием в регинарных лимфоузлах метастазов. Лимфодиссекция при раке желудка – это полное удаление всех лимфатических сосудов и узлов, а также прилегающей к ним жировой клетчатки.
Существует несколько вариантов этой хирургической процедуры, которые имеют непосредственную связь с объёмом подлежащих удалению тканей:
- D1. Вырезаются регионарные лимфатические коллекторы, находящиеся в связочном аппарате желудка.
- D2. Устранению подлежат как находящиеся в непосредственной близости, так и перигастральные коллекторы, относящиеся к вторичному метастазированию, и расположенные в червном стволе, по ходу артериальных ветвей.
- D3. Дополнительно к вышеперечисленным патологическим явлениям удаляются и расположенные вдоль аорты и пищевода лимфоузлы третьего этапа метастазирования.
Не так давно общепринятым объёмом данной процедуры, проводимой в обязательном порядке, считался вариант D1. В современной клинической практике при радикальных вмешательствах, позволяющих удалить поздний рак желудка, практически всегда выполняется лимфодиссекция в объёме D2, что способствует увеличению среди пациентов пятилетней выживаемости.
Паллиативная хирургия или операция для облегчения состояния больного
Если злокачественное новообразование основного пищеварительного органа не удалось своевременно обнаружить, и оно в своём развитии достигло последних, неоперабельных стадий, онкологи стараются облегчить состояние пациента и улучшить качество его жизни. Для этой цели и применяются паллиативные операции. При раке желудка проведение таких вмешательств называется симптоматическим и даёт возможность эффективно устранить те или иные опасные для жизни и очень тяжёлые симптомы, что временно облегчает состояние онкобольного.
В качестве паллиативной хирургии применяют:
- Циторедукционное вмешательство. Оно проводится для снижения общего количества аномальных клеток, что предупреждает распространение спровоцированного раковой опухолью разрушительного процесса в соседних с ней тканевых структурах и кровеносных сосудах. Ход операции подразумевает иссечение части желудка и удаление первичного очага патологии.
- «Прижигание» опухоли. При помощи высокочастотной или эндоскопической лазерной абляции уничтожаются мутировавшие клетки и снижаются риски возникновения прорывного желудочного кровотечения.
Выполнение таких симптоматических операций позволяет использовать облучение и химиотерапию при раке желудка, перешедшем в неоперабельную стадию. Также пациентам вводятся противоопухолевые вакцины и моноклональные антитела, что приводит не только к стабилизации болезни, но и удлинению периода жизни, которая будет протекать в более высоком качестве.
Виды операций
Последствия операции не всегда могут иметь положительный результат, и осложнения после нее весьма не редкой явление:
- Специальные стерильные условия операционной, обеззараженные поверхности и инструменты минимизируют риск заражения. Но в случае несоблюдения стерилизационных мер, возможно инфицирование раны. В этом случае наблюдается покраснение, нагноение шва, лихорадка, слабость.
- Внутренние кровотечения, опасно тем, что в отличие от внешних, проявляются не сразу.
Инвагинация
Вид основного заболевания, приведшего к резекции; Тип оперативного вмешательства и ход самой операции; Состояние больного в постоперационном периоде; Отсутствие/наличие осложнений; Правильное соблюдение режима и вида питания.
стадии заболевания;сложности проведенной резекции;соблюдения рекомендаций врача в период восстановления.
Осложнения и боли после резекции
После завершения операции лапароскопическим методом пациент будет находиться в стационаре приблизительно неделю. Несколько дней после вмешательства могут беспокоить болевые ощущения.
При необходимости доктор назначит обезболивающие препараты. Сразу после процедуры удаления опухоли больной может покушать, но пища должна быть мягкой.
К обычному питанию разрешается вернуться уже на 5 сутки после процедуры. Чтобы не спровоцировать развитие осложнений, нужно соблюдать щадящий режим – больше лежать и не совершать резких движений.
От секса нужно воздержаться в течение 6-8 недель после операции, необходимо избегать и физических нагрузок. Важно следить, чтобы участок кожи, где проводилась лапароскопия, был сухим и чистым.
Если пациенту проводилась колостомия или илеостомия, его инструктируют, как ухаживать за стомой без помощи специалиста. Если была сделана илеостомия, то по прошествии времени пациенту назначается еще одно хирургическое вмешательство, цель которого — соединить концы кишки.
Швы снимаются только врачом и не ранее, чем через 14 суток после лапароскопии. После больной получает направление в онкологию, чтобы пройти курс поддерживающей терапии.
Если после операции повышается температура тела (более 38 °С), нужно незамедлительно обратиться к врачу для выяснения причины.
высокий темп жизни; нерегулярное питание; некачественная пища.
Рассечение спаек
Установка катетера в центральную вену для контроля центрального венозного давления и парентеральных инфузий. Катетеризация мочевого пузыря для контроля диуреза. Установка назогастрального зонда.
Консервативная терапия является также и методом предоперационной подготовки (если операция все же потребуется).
Устранение препятствия. По возможности ликвидация заболевания, приведшего к данному осложнению. Максимально возможные действия для профилактики послеоперационных осложнений и рецидива.
Основные этапы операции и тактика хирурга
1. Анестезия. Обычно это – эндотрахеальный наркоз с миорелаксантами.
2. Доступ – чаще всего широкая срединная лапаротомия.
Послеоперационный этап у таких пациентов – очень важный момент лечения, не менее значимый, чем сама операция.
При появлении признаков кишечной непроходимости необходимо проконсультироваться с врачом-хирургом. Именно этот специалист определяет объем необходимых лечебных мероприятий.
В зависимости от причины развития, своевременности постановки диагноза, общего состояния пациента, оперативное вмешательство может быть срочным и плановым. Перед вмешательством проводят подготовку пациента. При плановой операции ее можно начинать дома, продолжать в больнице, при безотлагательной – в течение нескольких часов, в стационаре.
Операции по поводу кишечной непроходимости относятся к объемным вмешательствам с длительным послеоперационным периодом. Он определяется временем полного заживления раны и максимально возможным восстановлением организма.
Как проходит операция
Второе название гастрэктомии – экстирпация. Она проходит поэтапно под общей анестезией. Ход операции определяется степенью развития ракового процесса. Делается хирургический разрез, и перевязываются кровеносные сосуды. Потом орган отсекают от пищевода и кишечника в области присоединения. Кроме желудка удаляют регионарные лимфоузлы и сальники. Затем формируют соустье путём объединения пищевода и тонкого кишечника.
После операции проводят цитологическое исследование смывов. Отсутствие злокачественных клеток – показатель удачной операции. Оперативное вмешательство бесполезно при метастазах, если течение онкологического заболевания осложнено асцитом, эндокринными нарушениями. Туберкулёз также считается противопоказанием.
В предоперационный период пациент должен придерживаться диеты, режима дня, чтобы сбросить лишний вес. Следует отменить приём ацетилсалициловой кислоты и препаратов на её основе. День перед операцией нужно провести без пищи и очистить кишечник с помощью клизмы.
Инвалидность даётся после полного удаления желудка. Радикальная операция проводится, когда консервативное лечение не помогает. В результате выпадает важное звено в пищеварении, поэтому соблюдение диеты – жизненно необходимо для пациента.
Показания к операции
Инвагинация
Трахеостома – это искусственно созданное отверстие в шее с выведенной трубкой, которое устанавливается с целью воссоздания поврежденных функций дыхания человека. При нарушениях работы дыхательной системы, невозможности произведения самостоятельного акта вдоха-выдоха пациенту часто в экстренном порядке проводят стомирование трахеи.
Эпицистома выводится из мочевого пузыря на поверхность брюшной стенки с помощью специального катетера. Показаниями к назначению такой манипуляции является неспособность пациента к естественному мочеиспусканию по различным причинам. Бывают эпицистостомы временные и постоянные.
Колостома может носить временный или постоянный характер. Детям чаще всего проводят временную стому.
Недержание аноректального типа; Закупоривание кишечного просвета опухолевым образованием; Травматические повреждения толстокишечных стенок вроде огнестрельных или механических ранений; Тяжелые случаи толстокишечных патологий типа дивертикулита или ишемического колита, рака либо перитонита, полипоза и неспецифического язвенного колита, абсцессов стенок кишки с перфорацией и пр.
(если нет возможности провести радикальное вмешательство); При ректосигмоидной резекции, если после операции швы несостоятельны.
Как избежать последствий операции?
Необходимо отметить, что пациенты, которым выполнена резекция желудка, ощущают на себе проявление массы осложнений.
Последствия такого, достаточно серьёзного, хирургического воздействия могут быть очень опасными:
- Анастомозит. Воспалительный процесс, возникающий в месте соединения желудочной культи с 12-перстной кишкой.
- Анемия. Малокровие провоцируется постоперационным внутренним кровотечением.
- Перитонит. Воспаление брюшины.
- Летальный исход.
Чтобы данные осложнения после операции по типу дистальной субтотальной гастрэктомии не возникли, после удаления рака желудка, каждому конкретному пациенту назначается индивидуальная реабилитационная программа. Самым важным этапом её проведения считается ранний постоперационный период. Основными методами, позволяющими не допустить развития негативных последствий, предупредить рецидив рака желудка после операции и ускорить выздоровление человека, являются специально разработанная врачом диета, исключение каких бы то ни было физических нагрузок и ношение бандажа.
Также для улучшения состояния пациента в обязательном порядке проводится дальнейшая химиотерапия. После операции при раке желудка с помощью этого метода лечения устраняются все остаточные аномальные клетки, мигрирующие по организму с током крови. Такой тип лечения, хотя и провоцирует возникновение у человека большого количества побочных эффектов, признаётся медиками необходимым. Именно благодаря ему, при правильном назначении и проведении лекарственных процедур, возможно, избежать рисков развития побочных эффектов.
Органосохраняющие операции
Всё большее признание в мировой практике лечения больных с онкологическими заболеваниями завоёвывают органосохраняющие методы. Показанием к проведению такой операции является обнаружение ранних форм злокачественного новообразования.
Ранним раком желудка считают новообразование, поражающее подслизистый слой стенки желудка и его слизистую оболочку, вне зависимости от отсутствия либо наличия метастаз в лимфатических узлах.
При выявлении раннего рака желудка может быть возможным проведение органосохраняющего вмешательства – эндоскопической резекции пораженного участка слизистой оболочки в пределах здоровых тканей.
Методика проведения операции следующая. После того, как при помощи специальных красителей определяются чёткие размеры пораженной области, выполняется разметка планируемых границ вмешательства – она производится посредством электрокоагуляции. Далее хирург выполняет гидропрепаровку тканей (это необходимо для обеспечения лучшего визуального контроля слоёв и профилактики возможной перфорации стенки желудка). Через инструментальный канал эндоскопа проводится специальный электронож, после чего, под визуальным контролем, проводится резекция пораженного участка слизистой оболочки и подслизистого слоя – вплоть до мышечного слоя.
В реабилитационном периоде пациент находится под динамическим наблюдением врача, получая необходимую медикаментозную терапию. В сравнении со стандартным оперативным лечением, данный метод является более экономичным и менее инвазивным, а также позволяет сократить срок пребывания пациента в стационаре и ускорить реабилитацию.